Confiner l’eau permet de mieux comprendre sa réactivité
Dans nos sociétés en voie de décarbonation, le dihydrogène ou H2 pourrait être le vecteur énergétique du futur. En effet, il pourrait servir dans le futur de combustible pour certains transports (fret routier et maritime), ou de manière plus significative et directe comme réactif dans l’industrie chimie (production d’engrais, acier, etc.). Le dihydrogène est actuellement produit à plus de 95% par vaporeformage d’hydrocarbures, un procédé responsable d’émissions de CO2 et créant ainsi un hydrogène dit « gris ». Afin d’obtenir un hydrogène plus propre, ou « bleu », une alternative serait alors de le produire par électrolyse de l’eau alimentée par de l’électricité renouvelable.
L’application de cette solution à un niveau industriel, quoique prometteuse, reste pour l’instant limitée. La faute revient ici à des coûts encore trop importants ainsi qu’à des cinétiques de réactions trop lentes qui limitent les performances. En particulier, la cinétique de la réaction de réduction de l’eau H2O en H2 (2H2O + 2e- = H2 + 2 OH-) est connue pour être extrêmement sensible au milieu réactionnel, limitant par exemple les performances des électrolyseurs alcalins. Cependant, les mécanismes régissant cette réduction restent largement méconnus car H2O joue un double rôle, à la fois celui de solvant et celui de réactif. Il est ainsi difficile d’isoler et de distinguer ce qui va relever de l’un ou de l’autre.
Une équipe de chercheurs du RS2E, dirigées par Alexis Grimaud, chargé de recherche au Collège de France au sein du laboratoire de Chimie du Solide et Energie, et Mathieu Salanne, professeur à Sorbonne Université et membre du laboratoire PHENIX, propose une nouvelle approche méthodologique pour étudier en profondeur les mécanismes en jeu et comprendre les limites cinétiques. Leurs travaux ont été publiés dans la revue Nature Catalysis.
Confiner pour mieux isoler
Le principe de la méthode développée consiste à isoler les différentes interactions mises en jeu impliquant H2O, en l’étudiant dans un solvant organique qui joue alors le rôle de matrice inerte. Une fois confinée dans ce solvant, l’eau adopte des structures particulières. En effet, en modifiant la teneur en eau, en sel et en solvant organique, les chercheurs ont réussi à créer des nanodomaines d’eau (ou nanoréacteurs) dont la taille et la composition chimique peuvent être modulées. En fonction des propriétés de ces nanodomaines, les chercheurs peuvent contrôler indépendamment la force et le nombre des interactions H2O-H2O ou des interactions H2O-sel et comprendre leurs effets sur la cinétique de réaction. En confinant les molécules d’eau, les chercheurs peuvent ainsi établir une corrélation structure/réactivité et étudier séparément les effets à longue échelle qui relèvent de son rôle de solvant de ceux à courte échelle relevant de son rôle de réactif.
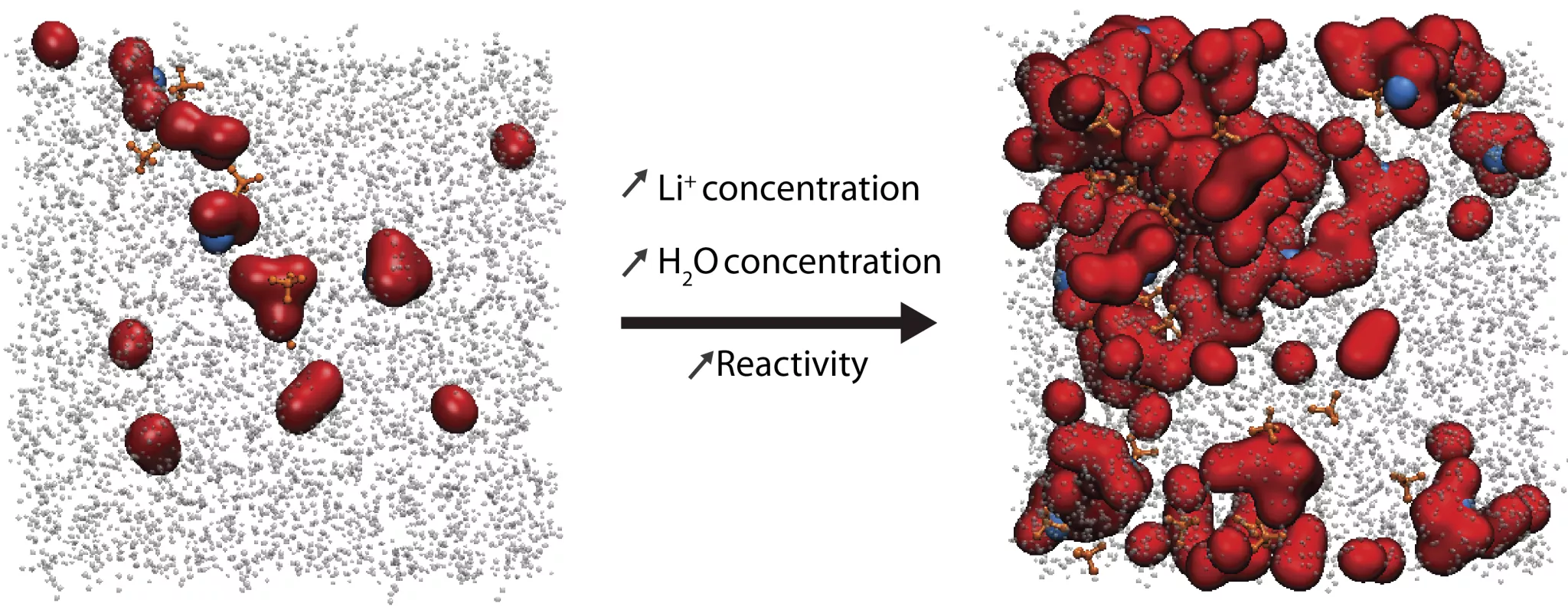
Figure 1 : En jouant sur les concentrations en eau et en cation, les expérimentateurs peuvent moduler la taille et la composition chimique des nanoréacteurs ainsi que leur réactivité.
Si cette approche, dans le cadre de l’électrolyse de l’eau, reste avant tout un outil méthodologique pour étudier l’impact des interactions en électrochimie, les résultats obtenus se révèlent néanmoins avoir un intérêt applicatif pour d’autres réactions d’intérêts. En effet, la maîtrise avancée de ce type de nanoréacteurs permet à un expérimentateur de fixer le potentiel auquel il souhaite faire réagir l’eau. Ceci pourrait se révéler utile pour obtenir une meilleure sélectivité pour d’autres réactions en milieu aqueux, ce qui est primordial pour l’électrosynthèse de produits organiques à haute valeur ajoutée ou pour d’autres réactions électro catalysée telles que la réduction du CO2 ou celle de N2 en NH3 (engrais).
Références :
Tuning water reduction through controlled nanoconfinement within an organic liquid matrix
Nicolas Dubouis et al.
Nature Catalysis, 27/07/20, DOI : 10.1038/s41929-020-0482-5
Contact : Alexis Grimaud, alexis.grimaud@college-de-france.fr et Mathieu Salanne, mathieu.salanne@sorbonne-universite.fr